Avances
NUEVO MEDICAMENTO
FDA aprueba primera opción semestral preventiva para el VIH
El inhibidor es la primera y única inyección preventiva
Jueves, 19 de junio de 2025, a las 11:19
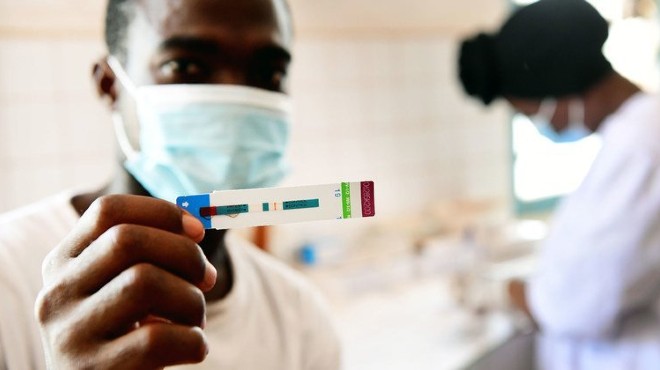
El fármaco fue probado en África. |
Redacción. Quito
La Administración de Alimentos y Medicamentos (FDA) de Estados Unidos ha aprobado el primer tratamiento semestral preventivo del VIH (Virus de la Inmunodeficiencia Humana) de venta en el país, informó el fabricante, Gilead Sciences.
El fármaco, lenacapavir, ha sido diseñado para reducir el riesgo de contraer el VIH por vía sexual en adultos y adolescentes que pesen al menos 35 kilogramos.
Daniel O'Day, presidente y director ejecutivo de Gilead, ha señalado en un comunicado que esta aprobación llega en un "momento clave en la lucha de décadas contra el VIH. Yeztugo nos ayudará a prevenir el VIH a una escala nunca vista. Ahora tenemos una manera de acabar con la epidemia de una vez por todas”.
Cabe señalar que este antirretroviral ya se usaba en pacientes con cuadros resistentes al virus que no responden a otros tratamientos, y, en un esperado ensayo clínico de fase 3 publicado en la revista NEJM y realizado con más de 5.000 personas el fármaco ha mostrado que también protegía de las infecciones en las 2.134 mujeres jóvenes de Sudáfrica y Uganda que recibieron dos inyecciones anuales del medicamento ya que ninguna se contagió.