Salud Pública
RESPUESTA OFICIAL
No queda claro el uso del remdesivir en pacientes ecuatorianos
¿El MSP está experimentando sin un responsable que lo asuma?
Lunes, 07 de septiembre de 2020, a las 16:44
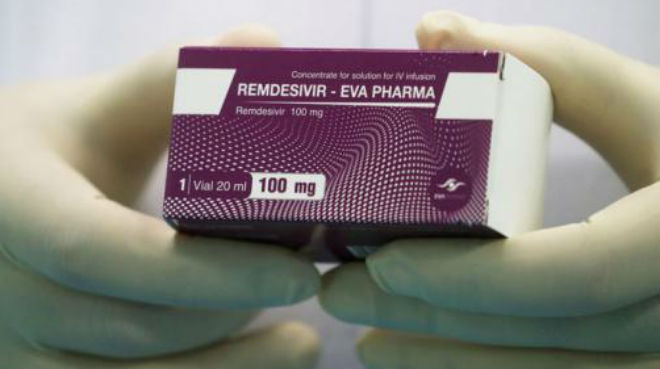
El fármaco no ha demostrado ser seguro y eficaz. |
Cristina Coello. Quito
Aunque Ecuador fue el primer país de la región en recibir una donación de 1.900 dosis de remdesivir y su uso era parte de una prueba “para medir sus resultados”, el Ministerio de Salud Pública (MSP) ha insistido en que su uso es compasivo, sin especificar quien se responsabiliza de gestionar posibles efectos adversos a pesar de tener un protocolo de uso del medicamento.
Tras el anuncio de la donación a inicios de agosto de 2020, EDICIÓN MÉDICA envió varias preguntas al MSP sobre el tema. Este medio mencionó que la evidencia científica alertaba de los riesgos y la pobre eficacia en CoVID19. La pregunta concreta fue: ¿En qué pacientes se usará?
La respuesta que hemos recibido es que “con base en el Acuerdo Ministerial 00043-2020 (aquí el documento), de fecha 13 de agosto de 2020”, donde se expidieron los lineamientos técnicos para el uso compasivo del remdesivir en paciente con CoVID-19”, los criterios de selección son:
“1. Pacientes con diagnóstico confirmado de CoVID 19 por RT-PCR; 2. Paciente con necesidad de ingreso a UCI a partir de la emisión de los presentes lineamientos o que se encuentre en UCI en un periodo no mayor a cinco (5) días.; 3. Paciente adulto; 4. Paciente con menos de doce (12) días desde el inicio de los síntomas; 5. Paciente que requiere ventilación mecánica invasiva y no invasiva; Paciente con distrés respiratorio”.
Mientras que, en los criterios de exclusión a recibir Remdesivir está cualquier paciente “que presente al menos una de las tres condiciones siguientes: “1. Falla hepática; 2. Falla renal y 3. Embarazo”.
¿Qué protocolo se usa? Fue la siguiente pregunta y la respuesta del MSP ha sido que en el Acuerdo Ministerial 00043-2020 (13 de agosto de 2020) se indican los “lineamientos técnicos” para el uso compasivo del remdesivir en paciente con CoVID19, en su Art. 11.- Esquema de administración, señala; Para administrar el medicamente remdesivir a los usuarios/pacientes que cumplan con los criterios de selección, esquema de tratamiento es el siguiente:
“Primero 200 mg (2 viales) dosis de carga en solución intravenosa el día 1; y, segundo: 100 mg (1 vial) en solución intravenosa una vez al día desde el día 2 hasta el día 5. El volumen total de administración puede ser de 250 ml o 500 ml de solución normal. La perfusión se puede administrar durante un periodo entre treinta (30) minutos y dos (2) horas”.
“Es necesario señalar el Art. 12.- Antes de la administración. - Es responsabilidad del médico tratante la verificación de que el paciente cumpla con los criterios de selección para recibir el medicamento Remdesivir”.
Al consultarles si era experimental el uso de remdesivir la respuesta fue que “el uso del medicamento se lo hará dentro del marco de la figura uso compasivo y obviamente se tendrá un seguimiento cercano de todos los beneficios y riesgos” de este.
No obstante, especialista en Farmacología, María Belén Mena, ha recordado que en ocasiones se usa medicamentos para fines que no han sido contemplados en su autorización inicial de comercialización y empleo, por parte de los organismos reguladores (para el Ecuador la ARCSA- Agencia Nacional de Regulación, Control y Vigilancia Sanitaria).
El remdesivir en Ecuador no tiene registro sanitario. Pero el que ha sido usado proviene de una donación, bajo estrictos protocolos con criterios de inclusión y exclusión. “Eso suena a ensayo clínico, pero no lo dicen. Darle un medicamento a un paciente para evaluar los resultados se llama experimento en cualquier parte del mundo”, ha considerado Mena.
Por ello, EDICIÓN MÉDICA también consultó al MSP si después de la donación el país compraría el fármaco y la respuesta fue que “se desconoce, pues depende de la evidencia científica que presente el medicamento y cumplir con los requisitos sanitarios para su comercialización en el país”.
Ante estas respuestas aún queda la duda de si el uso que se está dando, o se dio al remdesivir, en algunas unidades hospitalarias del MSP está dentro de un estudio científico.
Si no es un experimento el uso de ese fármaco, entonces “¿cuál es la independencia de los resultados? ¿cuál es la rigurosidad, pasó por un comité de bioética en salud?, ha cuestionado Mena.
La especialista ha considerado que es “terrible” no conocer si el país comprará o no el fármaco. “Queda la duda de qué va a pasar mañana luego de la donación y si el sistema de salud público está obligado a usar la supuesta donación”.
Eso deja entrever que también dependerá de los resultados de la evidencia que arroje el uso de un fármaco entregado por el fabricante. “Fue una donación con piola” y habrá que “tener cuidado” de las decisiones que a futuro se tomen respecto a la adquisición o no de este fármaco, ha sugerido.