Empresas
EN ADULTOS
La FDA aprueba completamente la vacuna contra la COVID-19 de Moderna
La de Pfizer recibió autorización el año pasado
Martes, 01 de febrero de 2022, a las 12:54
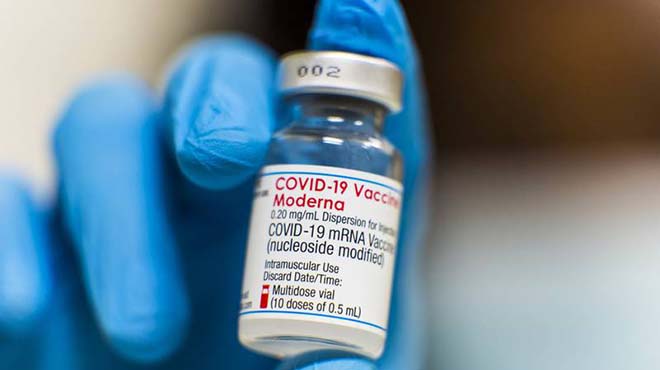
Es la segunda inyección totalmente aprobada. |
Redacción. Quito
La Administración de Alimentos y Medicamentos (FDA, por su sigla en inglés) de Estados Unidos ha dado su aprobación completa a la vacuna contra la COVID-19 de Moderna para personas de 18 años o más, lo que la convierte en la segunda inyección totalmente aprobada contra el coronavirus.
La vacuna fue autorizada para su uso de emergencia en Estados Unidos desde diciembre de 2020 y ahora se venderá bajo la marca Spikevax.
La vacuna contra la COVID-19 de Pfizer, que utiliza una tecnología similar, recibió el año pasado la aprobación completa en Estados Unidos para personas mayores de 16 años, tras obtener también primero la autorización de emergencia.
Casi 75 millones de personas han recibido ya la pauta de dos dosis de la vacuna de Moderna en Estados Unidos, según datos de los Centros para el Control y la Prevención de Enfermedades (CDC).
“El público puede estar seguro de que Spikevax cumple los elevados estándares de seguridad, eficacia y calidad de fabricación que la FDA exige a cualquier vacuna aprobada para su uso en Estados Unidos”, ha señalado Janet Woodcock, comisionada subrogante de la FDA, en un comunicado.
La vacuna de Moderna está autorizada para su uso en más de 70 países, incluidos Canadá y la Unión Europea.
En junio de 2021, la empresa solicitó la autorización de su vacuna para su uso en jóvenes de 12 a 17 años, pero la FDA aún no ha respondido.
Tanto la vacuna de Moderna como la de Pfizer/BioNTech se han relacionado con casos raros de inflamación del corazón llamada miocarditis, especialmente entre hombres jóvenes.
Algunos estudios han sugerido que la vacuna de Moderna tiene más probabilidades de causar este efecto secundario que la de Pfizer/BioNTech.
En octubre, Moderna informó a la FDA estaba evaluando el riesgo de miocarditis tras la vacunación y que la revisión estaba retrasando la autorización de su vacuna en adolescentes.