Salud Pública
ALERTA SANITARIA
Retiro del mercado europeo de Valsartán no afecta a pacientes de Ecuador
El medicamento no se encuentra registrado en las bases locales
Jueves, 12 de julio de 2018, a las 17:37
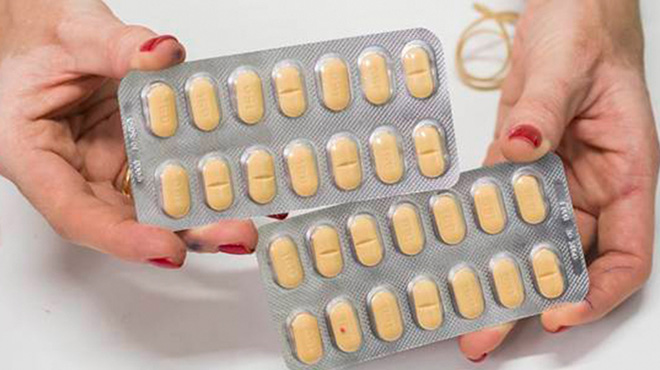
El medicamento es retirado en España. |
Redacción. Quito
La Agencia Nacional de Regulación, Control y Vigilancia Sanitaria (Arcsa) ha informado que una alerta emitida por la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) sobre el Valsartán no afecta a los pacientes en el Ecuador, ya que no se encuentra registrado en las bases de medicamentos locales.
AEMPS había advertido a los a los profesionales de salud, instituciones, establecimientos farmacéuticos y al público en general la detección de una impuresza (N-Nitrosodimetilamina -NDMA) en el principio activo Valsartán, fabricado por Zhejing Huahai Pharmaceutical Co. (Ltd (BS 1) Channan Site, RC-317016 (China).
Dicha impureza se ha generado como consecuencia de un cambio en el proceso de fabricación autorizado por el EDQM (por sus siglas en inglés de la Dirección Europea de la Calidad de los Medicamentos).
Esta alerta afecta a múltiples países europeos principalmente, ya que el medicamento producido por ese fabricante tiene varias presentaciones.
En España, tras recibir la correspondiente investigación se procedió a ordenar la retirada de los medicamentos afectados. En estos momentos las autoridades europeas de medicamentos están trabajando con Zhejiang Huahai para resolver la situación tan rápido como sea posible, evaluando el posible riesgo asociado.
Arcsa continúa con el monitoreo diario de alertas internacionales e información de seguridad en las páginas web de las Agencias Reguladoras de Referencia a nivel mundial y de ser necesario se actualizará la información, ha explicado la institución en un comunicado.
El principio activo
Valsartán es un principio activo antagonista del receptor de la angiotensina-II que se utiliza para tratar la hipertensión arterial. Se encuentra disponible solo o en combinación con otros principios activos.