Avances
TRAS PANDEMIA
La EMA allana el camino hacia los ensayos clínicos coordinados en emergencias de salud pública
Se publicó un informe que recopiló ideas y sugerencias
Miércoles, 02 de agosto de 2023, a las 12:28

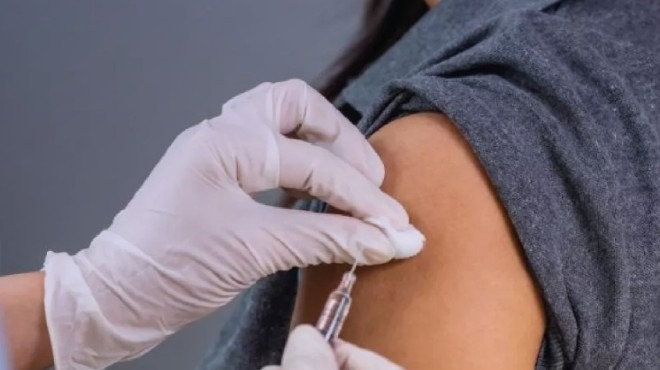
Superar barreras y desafíos durante la COVID-19 fue un reto. |
Redacción. Quito
La Agencia Europea del Medicamento (EMA) ha publicado un informe sobre las posibles acciones para mejorar la forma en que se establecen los ensayos clínicos en la Unión Europea (UE) durante emergencias de salud pública.
El tema fue analizado en un taller organizado por el Grupo de trabajo de emergencia (ETF) de la EMA y la Comisión Europea (CE), donde se plantearon acciones encaminadas a establecer ensayos clínicos (multinacionales) y abordar de manera integral las barreras y desafíos experimentados durante la pandemia de COVID-19 y el brote de viruela símica.
Según un comunicado oficial de la EMA, esto permitirá recopila de forma rápida evidencia suficiente y de alta calidad para respaldar la toma de decisiones por parte de las autoridades sanitarias en toda la UE.
Las discusiones del taller enfatizaron “la necesidad de estudios más amplios en varios países europeos, el reclutamiento más rápido y la entrega de resultados concluyentes con plazos acelerados durante una emergencia de salud pública”, ha señalado el comunicado.
Dos áreas de acciones
La una propuesta se ha centrado en la tramitación y aprobación regulatoria de grandes ensayos clínicos multinacionales en la UE durante emergencias de salud pública.
Eso incluiría, por ejemplo, mejorar la coordinación entre reguladores y comités de ética dentro y entre los Estados miembros, acelerar la evaluación y autorización de las solicitudes de ensayos clínicos y explorar flexibilidades en la implementación del Reglamento de ensayos clínicos y facilitar el uso del Sistema de Información de Ensayos Clínicos (CTIS) de la UE.
La segunda área está relacionada al financiamiento y la asignación eficiente de recursos para ensayos clínicos durante emergencias en la UE, “incluido el establecimiento de un Comité de Coordinación para apoyar la priorización de ensayos, mecanismos mejorados para identificar y clasificar compuestos prometedores, movilización de mecanismos y medidas de financiación de la UE y los Estados miembros para ayudar a acelerar la contratación de sitios de ensayos clínicos”
La EMA ha enfatizado en la necesidad de hacer de Europa “un lugar mejor para la investigación”.
#JustPublished!
— EU Medicines Agency (@EMA_News) July 25, 2023
Proposed actions to improve the way clinical trials are set up and conducted in the ?? during public health emergencies.
Read the report: https://t.co/zryO5hLwsL#PublicHealth #ClinicalTrials pic.twitter.com/RvSBn9YIbR